Tout ce qui t’entoure est fait de matière : l’air, l’eau, les roches, les plantes, ton corps. Cette matière est constituée d’unités très petites appelées atomes. Chaque atome possède un noyau au centre, formé de protons et de neutrons, et des électrons qui se déplacent autour. Les atomes peuvent s’associer pour former des molécules, puis des matériaux et des objets plus complexes. Ce principe est valable sur Terre comme dans l’Univers : étoiles, planètes et autres astres sont eux aussi composés d’atomes. Comprendre l’atome, c’est comprendre la structure de la matière, ici et ailleurs dans le cosmos.
Qu’est-ce que la matière ?
La matière, c’est tout ce qui :
- occupe un espace (prend de la place),
- et possède une masse (on peut la peser ou la mesurer).
Une pierre, une feuille, une goutte d’eau, l’air dans un ballon, ta trousse : ce sont des exemples de matière.
Même si tu ne vois pas l’air, tu peux constater qu’il existe : un ballon se gonfle, devient tendu, plus “dur” au toucher. L’air qu’il contient occupe un volume : c’est donc de la matière.
Dans l’Univers, c’est la même idée : une planète, une étoile ou un astéroïde sont aussi des masses de matière, mais à une échelle beaucoup plus grande.
Les briques de base : les atomes
Si on pouvait zoomer de plus en plus sur n’importe quel objet :
- d’abord on verrait sa surface,
- puis des fragments plus petits,
- puis, à une échelle encore plus réduite, on finirait par atteindre les atomes.
Les atomes sont les unités de base de la matière. Il en existe différents types, par exemple l’hydrogène, l’oxygène, le carbone, le fer, etc. Chaque type d’atome se distingue par le nombre de protons dans son noyau : par exemple, un atome d’hydrogène possède 1 proton, un atome d’oxygène en possède 8. En les combinant de différentes façons, on obtient une grande variété de substances.
Quelques exemples simples :
- certaines roches contiennent beaucoup d’atomes d’oxygène et de métaux comme le fer ;
- ton corps contient en grande partie des atomes de carbone, d’oxygène et d’hydrogène ;
- l’air qui nous entoure contient surtout de l’azote et de l’oxygène ;
- dans les étoiles, on trouve surtout des atomes d’hydrogène et d’hélium.
Même très loin dans l’espace, on retrouve donc les mêmes unités fondamentales : les atomes.
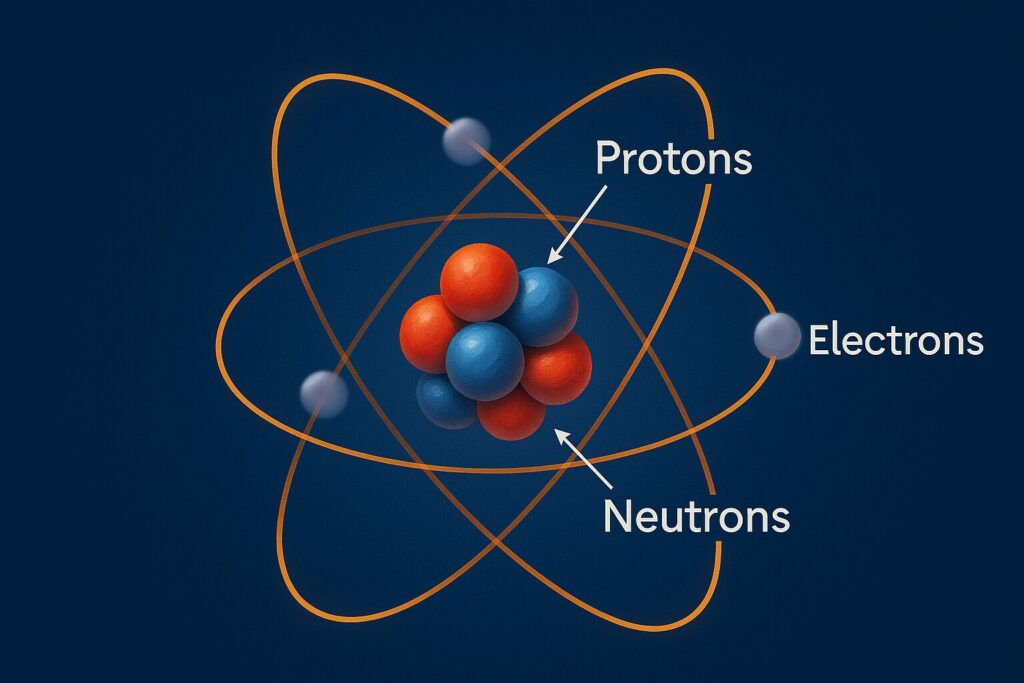
À l’intérieur d’un atome
Un atome n’est pas plein comme une bille de verre. Il comporte deux grandes parties :
- Le noyau
situé au centre de l’atome ; très petit, mais il concentre presque toute la masse de l’atome ; composé de protons et de neutrons. - Les électrons
très légers ; se déplacent autour du noyau ; occupent une région beaucoup plus étendue que le noyau lui-même.
Pour se faire une première idée, on compare parfois l’atome à un système solaire en modèle réduit :
- le noyau joue le rôle du “Soleil” au centre,
- les électrons sont comme des “planètes” qui évoluent autour.
Ce modèle est simplifié par rapport à ce que décrit la physique moderne, mais il reste utile pour comprendre les rôles des différentes particules.
Protons, neutrons, électrons : qui fait quoi ?
Dans un atome, on distingue trois types de particules principales :
- Protons
situés dans le noyau ; portent une charge électrique positive ; comme on l’a déjà vu, le nombre de protons dans le noyau définit le type d’atome (par exemple : 1 proton → hydrogène ; 8 protons → oxygène). - Neutrons
eux aussi dans le noyau ; neutres : ils ne portent pas de charge électrique ; ils contribuent à la stabilité du noyau. - Électrons
en mouvement autour du noyau ; portent une charge électrique négative ; sont beaucoup plus légers que les protons et les neutrons.
À retenir :
- proton → charge positive,
- neutron → pas de charge,
- électron → charge négative.
Dans un atome ordinaire (neutre), le nombre de protons est égal au nombre d’électrons. Les charges positives des protons et les charges négatives des électrons se compensent, ce qui rend l’atome globalement neutre.
Un atome, c’est surtout du vide
Un point important, mais un peu surprenant : un atome est constitué en grande partie de vide.
Si l’on agrandissait un atome de manière imaginaire :
- le noyau aurait la taille d’un petit pois placé au centre d’un grand stade ;
- les électrons se trouveraient très loin autour, près des tribunes ;
- entre le noyau et les électrons, il y aurait essentiellement du vide.
Pourtant, tu ne passes pas au travers de ta chaise ou de la table. Cela s’explique par des forces qui agissent entre les particules, un peu comme les forces entre deux aimants qui se repoussent ou s’attirent : elles empêchent les objets de se traverser, même si, à l’échelle microscopique, il y a beaucoup d’espace vide.
Dans certains astres extrêmement denses (étoiles à neutron), la matière peut être beaucoup plus comprimée que dans la matière “classique”. Pour comprendre ces cas particuliers, il est essentiel de bien maîtriser d’abord la structure d’un atome ordinaire.
Des atomes aux molécules, puis aux objets
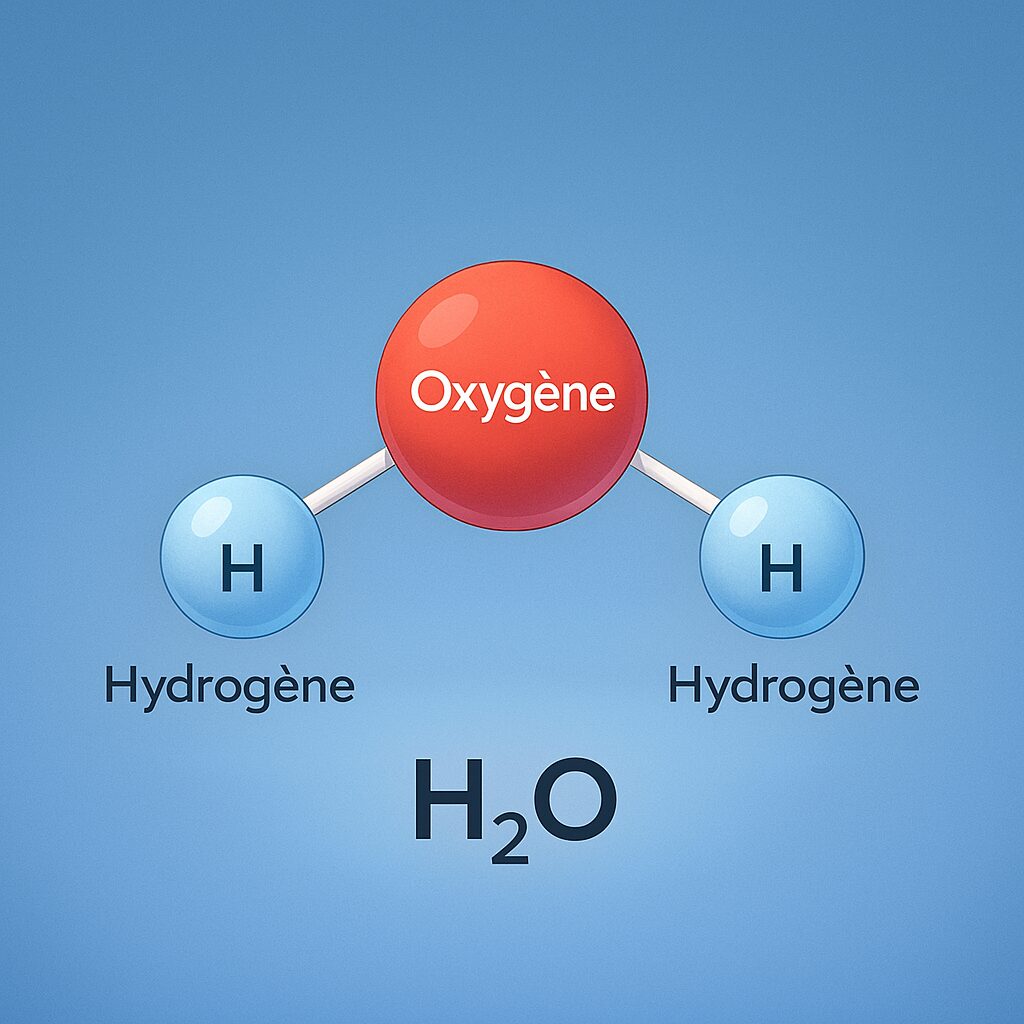
Les atomes peuvent s’associer entre eux. Lorsqu’ils se lient, ils forment des molécules. Ces molécules constituent ensuite les différents matériaux et substances.
Quelques exemples :
- Une molécule d’eau (H₂O) : 2 atomes d’hydrogène + 1 atome d’oxygène.
- L’air que tu respires contient de l’oxygène, indispensable à la vie.
- Le gaz carbonique (dioxyde de carbone) que nous rejetons en respirant contient du carbone et de l’oxygène.
En changeant la manière dont les atomes sont organisés et liés, on obtient des substances très différentes : sucre, sel, plastiques, métaux, tissus, roches, etc.
Sur une planète, dans un astéroïde ou à la surface d’une lune, ce sont toujours des atomes et des molécules qui constituent les roches, les glaces ou les gaz présents.
Atomes et états de la matière
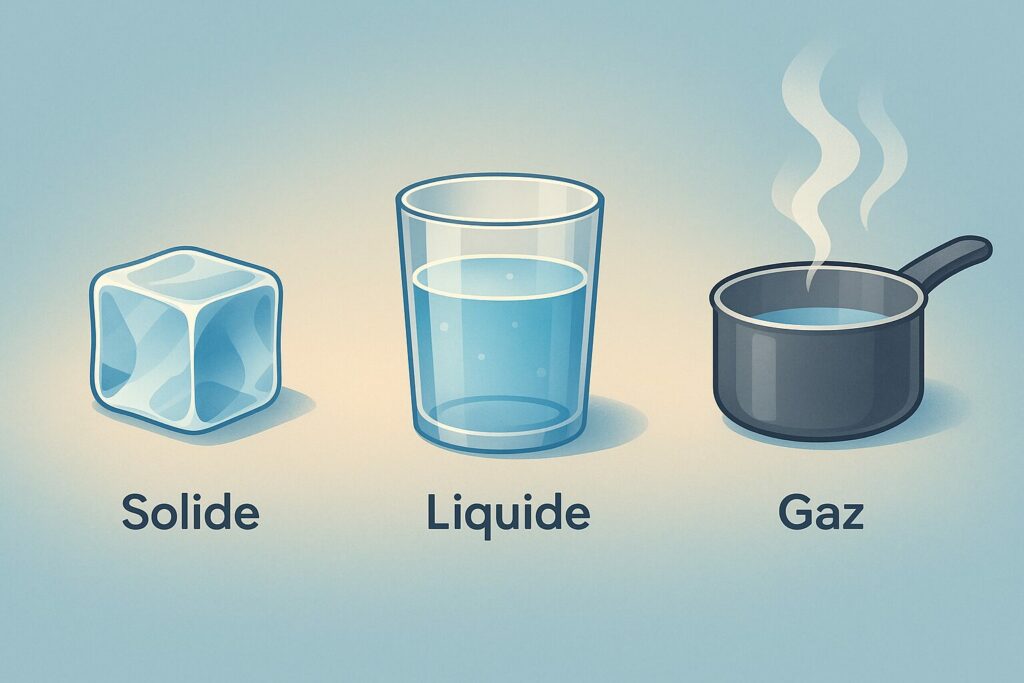
La matière peut se présenter sous trois grands états :
- Solide : forme bien définie (ex. un caillou, un livre, un glaçon).
- Liquide : prend la forme du récipient (ex. eau, huile, jus).
- Gaz : occupe tout l’espace disponible (ex. l’air dans une pièce, la vapeur d’eau).
À l’échelle des atomes et des molécules :
- dans un solide, ils sont très proches et assez bien organisés ;
- dans un liquide, ils restent proches, mais peuvent se déplacer et “glisser” les uns par rapport aux autres ;
- dans un gaz, ils sont plus éloignés et se déplacent rapidement dans toutes les directions.
Quand on chauffe une matière, les atomes et les molécules reçoivent de l’énergie, bougent davantage, et l’état peut changer : un solide peut fondre (glaçon → eau liquide), puis un liquide peut s’évaporer (eau → vapeur).
Dans l’Univers, on retrouve aussi ces états : glaces solides sur certaines lunes, océans liquides sur certaines planètes, et de grandes masses de gaz dans les étoiles et les nuages interstellaires.
En résumé
- La matière est tout ce qui a une masse et occupe un volume, sur Terre comme dans l’Univers.
- Elle est formée d’unités très petites, les atomes.
- Un atome possède un noyau (avec protons et neutrons) et des électrons qui se déplacent autour.
- Protons = charge positive, électrons = charge négative, neutrons = neutres.
- Le nombre de protons dans le noyau détermine le type d’atome (hydrogène, oxygène, carbone, fer, etc.).
- À l’échelle de l’atome, il y a beaucoup de vide, même si la matière nous paraît compacte.
- Les atomes s’assemblent en molécules, qui composent toutes les substances : roches, eau, air, êtres vivants… mais aussi étoiles, planètes et autres astres.

